Los avances en biotecnología han permitido desarrollar innovadoras terapias que van más allá de los medicamentos tradicionales formulados con químicos, como la aspirina o el paracetamol.
Los biofármacos o medicamentos biológicos —que incluyen proteínas recombinantes, anticuerpos monoclonales, vacunas— se elaboran mediante la ingeniería genética, y se usan para tratar ciertos tipos de cáncer, enfermedades inflamatorias o autoinmunes, entre otras. Se estima que más de 350 millones de personas en el mundo han sido tratadas con biológicos en casos de cáncer, enfermedad renal, algunos tipos de artritis, psoriasis, desórdenes del crecimiento y la enfermedad inflamatoria intestinal.
Los anticuerpos monoclonales para tratar el cáncer son moléculas diseñadas para “reconocer” células tumorales. Algunos estimulan el sistema inmune para destruirlas; otros interfieren con las proteínas que están involucradas en el desarrollo y proliferación de estas células. Ya hay algunos aprobados y otros están todavía a prueba en ensayos clínicos.
Pese a su potencial terapéutico, un inconveniente de los medicamentos biológicos es que, debido a que su fabricación o bioprocesamiento es más complejo, su costo es más elevado, lo que en algunos casos dificulta su accesibilidad para los pacientes (influyendo en la adherencia al tratamiento), la cobertura de los seguros o de los sistemas públicos de salud.
Además, aunque las drogas biológicas y las proteínas terapéuticas pueden inducir una respuesta del sistema inmune del paciente (inmunogenecidad), esta puede variar de una persona a otra, e incluso en el mismo paciente a lo largo del tiempo.
La inmunogenecidad es determinada por varios factores, entre ellos la estructura de la proteína, el proceso de producción, el historial del paciente y la vía de administración. Aún es difícil predecir cuál será el resultado de un producto respecto a la inmunogenecidad, para eso se hacen estudios clínicos.
A esto se suma la controversia sobre los potenciales efectos de la intercambiabilidad entre medicamentos biológicos, y al cambio y/o sustitución de un biológico por un “biosimilar”, un tema en el cual la farmacovigilancia es importante.
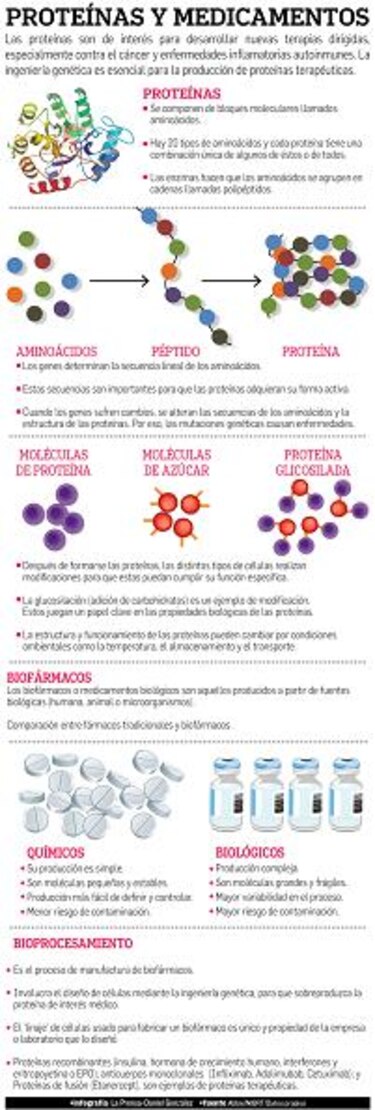
PROTEÍNAS
Muchas enfermedades no infecciosas tienen una base genética. En algunos casos, el paciente puede haber heredado una mutación que afecta la producción de alguna proteína específica en sus células, lo cual conlleva un mal funcionamiento de su organismo. El ADN también puede dañarse por factores externos, como el hábito de fumar o la exposición solar sin protección.
En los últimos años hay un gran interés por las proteínas como base para desarrollar nuevos fármacos, y se están haciendo muchas investigaciones relacionadas con los procesos que ocurren dentro de las células, la formación y modificación de proteínas, pero la ciencia aún no lo entiende todo.
Las proteínas de un fármaco biológico son inestables y su estructura puede desnaturalizarse si no se tiene cuidado con la temperatura, almacenamiento y transporte. 
BIOFÁRMACOS
Estos productos son derivados de una fuente biológica, como células humanas, de animales, bacterias, levaduras, etc. A diferencia de un fármaco químico, que consta de moléculas pequeñas y estables, los medicamentos biológicos son moléculas más grandes, pesadas y complejas, que se inyectan, son más susceptibles a la contaminación y se elaboran mediante biotecnología.
El bioprocesamiento requiere instalaciones con un diseño especial, medidas extremas de bioseguridad, mucho papeleo y personal altamente capacitado.
Durante un taller en el Instituto Nacional para la Investigación y Entrenamiento en Bioprocesamiento (NIBRT, por sus siglas en inglés), en Irlanda, coordinado por la empresa Abbvie, comunicadores de diferentes países pudieron conocer los laboratorios y aprender sobre el bioprocesamiento.
Los voceros explicaron que lo principal para una compañía que hace biofármacos es desarrollar su propio linaje celular, para crear un sistema de producción industrial de la droga que buscan.
Partiendo de su fuente biológica original, establecen un “banco maestro” de células generadas por ingeniería genética para producir una proteína específica. Estas células se comportan como pequeñas “fábricas de proteínas”.
Las células son cultivadas en medios ricos en nutrientes. A medida que van proliferando, se llevan a recipientes o biogeneradores de distintos tamaños, según la cantidad que se vaya a producir. Cuando el cultivo termina, las células se trabajan en diferentes partes de la planta. Se usan centrifugadoras y filtros para removerles los contaminantes y purificarlas, y se les hacen diversas pruebas. El proceso de envasado en viales es muy delicado y requiere de personal muy especializado que debe cumplir un estricto protocolo de seguridad.
Dado que el banco maestro de células es crítico para la producción de las moléculas, muchas compañías tienen bancos en diferentes instalaciones. Incluso, producen un segundo banco de células para trabajar.
Distintas compañías pueden usar el mismo tipo de células para trabajar, pero el linaje celular de cada una será único y propiedad de la empresa que lo creó.
BIOSIMILARES Y ORIGINADORES
Un fármaco biosimilar no es lo mismo que un “genérico”. Tampoco es idéntico a una droga biológica “originadora” debido a que el proceso para su elaboración es inverso y en él se usa un linaje celular distinto. Aunque sea similar a un fármaco originador, puede variar en su formulación, pureza, empaque, estabilidad y tiempo de vida almacenado.
Desde la perspectiva científica, las diferencias deben ser sustentadas cuando se trata de seguridad y eficacia. Los biosimilares requieren de su fabricante más pruebas analíticas, pero menos ensayos clínicos. Los países manejan diferentes definiciones para los biosimilares, y en función de eso, también hay normas relativas a su intercambiabilidad o sustitución.
A veces los pacientes cambian su medicina biológica por otra debido a razones médicas, como cuando no obtienen una respuesta adecuada. Otra razón, no médica, sería por el precio o porque no está disponible. Los pacientes podrían experimentar varios cambios entre estos medicamentos y el panorama se volverá más complejo en la medida que surjan más biosimilares en relación a un originador, y que se den múltiples cambios de uso entre ellos. Los estudios científicos y la fármacovigilancia juegan un rol crucial para garantizar que los pacientes reciban un tratamiento oportuno, seguro y efectivo. Cuando se trata de medicinas biológicas y biosimilares, es importante la interacción entre el sector farmacéutico y el de salud, los tomadores de decisiones, reguladores y los pacientes, para discutir temas como los costos, el conocimiento de los médicos sobre nuevos productos, la estandarización de normas, la cobertura que brinden los seguros médicos y sistemas públicos de salud y los efectos de un potencial desabastecimiento para los pacientes.




